2.10.2010, 22 h : Vier
Schüler haben Antworten gemailt, und sie reichen zum Zusammenstellen dieser
Antwortseite. Damit ist die Liste für die vier Fragen zum Thema 02
Dampf, Nebel, Gas, Rauch: Drei verschiedene Dinge
geschlossen.
1. Was hat Dampf mit Nebel zu tun? Nebel ist im Grunde genommen sichtbarer Wasserdampf. Wasserdampf ist ein Gas, nämlich der gasförmige Zustand von Wasser und daher in seiner reinen Form unsichtbar. Kühlt es allerdings in der Luft wieder ab, so entstehen sogenannte Aerosole, das sind kleine Partikel (hier flüssig), die in der Luft "schweben". Sie sind dann als Nebel sichtbar. Quelle:http://www.cosmiq.de/qa/show/1530767/Was-ist-der-Unterschied-zwischen-nebel-und-dampf/ 2. Rauch ist etwas ganz anderes. Was nämlich?
Rauch ist ein meist durch Verbrennungsprozesse entstehendes Aerosol in feinstverteilter (oft kolloidaler) Form aus Abgasen, Staubpartikeln (Ruß, Flugasche, Unverbranntes) und Nebeltröpfchen (Wasser, Öldämpfe, Säuredämpfe). Im engeren Sinn wird mit Rauch ein Gemisch aus einer festen in einer gasförmigen Phase bezeichnet. Rauch sind kleine schwebende Festpartikel in der Luft. Quelle:http://de.wikipedia.org/wiki/Rauch Beide Antworten wurden gemailt von M.S.
...................................................
Die folgenden Antworten wurden gemailt von D.G. Kursiv hat der Lehrer ein bisschen kommentiert::
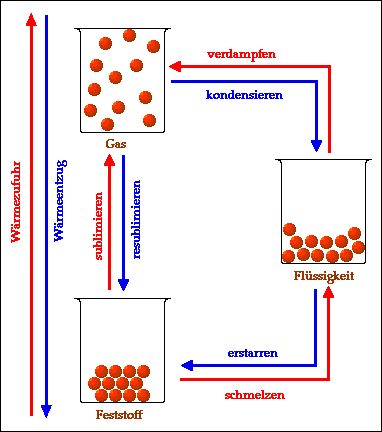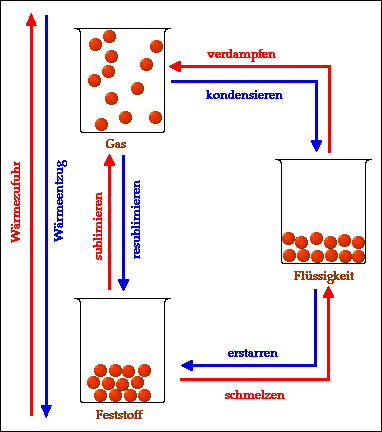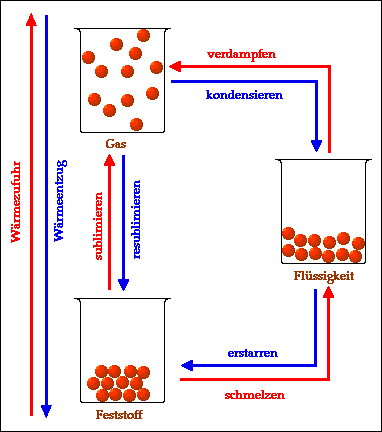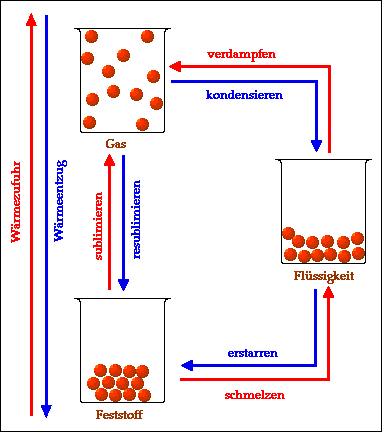 |
Zusammenfassend kann man die
verschiedenen Übergänge zwischen Aggregatzuständen wie folgt
darstellen: Durch Wärmezufuhr (erwärmen) werden folgende Übergänge möglich: - schmelzen (Übergang von fest zu flüssig) - verdampfen (Übergang von flüssig zu gasförmig) - sublimieren (Übergang von fest zu gasförmig). Durch Wärmeentzug (abkühlen) werden folgende Übergänge möglich: - erstarren (Übergang von flüssig zu fest) - kondensieren (Übergang von gasförmig zu flüssig) - resublimieren (Übergang von gasförmig zu fest). Hier noch ein Link zum
"Dreieck der Aggregatzustände": |
1. Was hat Dampf mit Nebel zu tun?
Eine Art Nebel, der auf der Wasseroberfläche auftritt und erscheint als
Dampf oder kondensierter Wasserdampf. Diese Art von Nebel entsteht, wenn
sehr kalte Luft über einer wärmeren Wasseroberfläche verläuft und
vermischt sich mit der warmen Luft dort. Für den Nebel zu kommen, ist die
Temperatur niedriger Regel um den Gefrierpunkt oder niedriger, und es
sollte eine deutliche Inversion in der Luft, bevor es über das Wasser
bewegt.
Tja. Das hat wohl der
Babelfisch aus dem Englischen übersetzt. Können wir so nicht nutzen.
http://www.youtube.com/watch?v=zCdcayc1U8w
Das ist klassische Musik mit romantischen Landschaftsbildern, 1.50 min
kurz. ja, warum nicht.
2. Rauch ist etwas ganz anderes. Was nämlich?
Rauch ist ein meist durch Verbrennungsprozesse entstehendes Aerosol in
feinstverteilter (oft kolloidaler) Form aus Abgasen, Staubpartikeln (Ruß,
Flugasche, Unverbranntes) und Nebeltröpfchen (Wasser, Öldämpfe, Säuredämpfe).
Im engeren Sinn wird mit Rauch ein Gemisch aus einer festen in einer gasförmigen
Phase bezeichnet.
Umgangssprachlich wird dichter, undurchsichtiger und gegebenenfalls dunkler
Rauch als Qualm bezeichnet. Rauch/Abgas aus Bränden nennt man auch
Brandgas. Rauch und Abgas aus technischen Verbrennungsanlagen wird auch als
Rauchgas bezeichnet.
Rauch ist in der Regel ein Schadstoff für Mensch und Umwelt. Im Gegensatz
zu einem unkontrollierten Feuer (Brand) findet kontrollierte Verbrennung
daher normalerweise in geschlossenen Behältern (wie Maschinen, Öfen und
Lampen) statt und die Rauchgase werden durch eine entsprechende Öffnung
(Auspuff, Schornstein, Saugzug) kontrolliert abgeleitet. Bei industriellen
Anlagen wird das Rauchgas zuvor gereinigt, sodass neben Stickstoff praktisch
nur noch Wasserdampf und Kohlenstoffdioxid den Schornstein verlassen.
http://www.myvideo.de/watch/4650284/Chemische_Reaktion_Herstellung_von_Rauch
Flüssigkeit 1, Flüssigkeit
2. Nichts passiert. Pulver dazu: Nebel steigt auf. Verhält sich wie kalter
Kohlendioxid-Nebel. Wir schauen in den Infos zum Film nach: Da steht NICHTS.
Das ist wenig.
3. Wir schauen in einen blauen Himmel mit einigen Wolken. Welches Gas ist
da, und welcher Dampf?
Eine Wolke ist eine Ansammlung von sehr feinen Wassertröpfchen (Nebel) oder
Eiskristallen. Die Wassertröpfchen bilden sich um Kondensationskerne herum,
wenn die relative Feuchtigkeit der Luft 100 % geringfügig, um höchstens 1
% übersteigt. Dies kann entweder durch Abkühlung der Luft beim Aufsteigen
(Thermik, Aufgleiten an anderen Luftschichten oder am Berghang) oder durch
Durchmischen zweier Luftmengen geschehen (Richard Mollier). Beim
Kondensieren wird die Verdampfungswärme des Wassers frei, welche das Abkühlen
bei weiterem Aufsteigen der Luft abschwächt. Dadurch kann die Luft in größere
Höhen steigen. Bei ruhiger Luft und wenigen Kondensationskernen kann es zu
einer Übersättigung der Luft mit Wasserdampf kommen. Obwohl der relative
Wassergehalt dann deutlich mehr als 100 % beträgt, kommt es noch zu keiner
Kondensation. Der Wassergehalt muss erst weiter zunehmen, bevor er
kondensiert. Bei einer Lufttemperatur unter -10 °C können sich an den
Kondensationskernen Eiskristalle (Schneeflocken) durch Resublimation bilden.
Kondensationskerne sind elektrisch geladen und haben eine Größe von 1 nm
bis 1000 nm. Sie entstehen durch die Natur und kosmische Strahlung (Beispiel
Nebelkammer). Auch private Haushalte, Industrie und Landwirtschaft können
beteiligt sein. Nach Beginn der Kondensation kondensiert immer mehr
Wasserdampf an dieser Stelle, bis es zu einem sichtbaren Nebeltröpfchen
wird. In der meteorologischen Systematik werden die Wolken den Hydrometeoren
zugerechnet.
http://www.mrbbc.org/files/de/cloudlevels.htm
Nett gebastelte
Javascript-Seite mit 10 Wolkenfotos. Echt gut erklärend. Will man eine
Wolke größer holen durch Klick drauf, kommt stattdessen die
Wikipedia-Seite zum Wolkentyp. Auch ok.
Dann linke ich also ergänzend zu "Wollkenfotos satt":
http://www.wolkenatlas.de/
4. Aggregatzustände: Welche gibt es, und wie heißen die Übergänge
zwischen ihnen?
http://www.youtube.com/watch?v=nG69b0Lxwno
Opa erzählt den Enkeln, was
Spaß macht. Erst mal eine Minute Anlauf, aber dann wird in der Küche
gekühlt und gekocht. In der zweiten Minute dann der Spiegel, sehr richtig,
und zum Schluss der Sicherheitshinweis. Super schlicht alles, aber so kann
man mal starten.
Als Aggregatzustände bezeichnet man qualitativ verschiedene, temperatur-
und druckabhängige physikalische Zustände von Stoffen. Die Abhängigkeit
des Aggregatzustandes beziehungsweise des in der Thermodynamik enger
gefassten Begriffs der Phase von diesen Zustandsgrößen wird üblicherweise
in einem Phasendiagramm dargestellt.
Es gibt drei klassische Aggregatzustände:
• fest - in diesem Zustand behält ein Stoff im Allgemeinen sowohl Form
als auch Volumen bei, siehe Festkörper
• flüssig - hier wird das Volumen beibehalten, aber die Form ist unbeständig
und passt sich dem umgebenden Raum an, siehe Flüssigkeit
• gasförmig - hier entfällt auch die Volumenbeständigkeit, ein Gas füllt
den zur Verfügung stehenden Raum vollständig aus, siehe Gas
Bei Feststoffen unterscheidet man auch nach anderen Merkmalen:
• kristallin - ein spröder Feststoff, der seine Form nicht verändert.
Seine Bausteine, die Kristalle, weisen eine Fernordnung auf.
• amorph - ein Feststoff, der lediglich durch eine Nahordnung
ausgezeichnet ist, siehe amorphes Material
Versuch 1:
Ein Stück Eis wird langsam erhitzt. Der Feststoff Eis geht bei diesem
Vorgang langsam in die Flüssigkeit Wasser über. Misst man die Temperatur,
so bemerkt man, dass diese konstant bei 0°C bleibt, so lange ein Eis-Wasser-Gemisch
vorliegt. Diese Temperatur nennt man die Schmelztemperatur des Eises.
Bringt man die Flüssigkeit durch Erhitzen zum Kochen, dann geht die Flüssigkeit
Wasser in einen gasförmigen Zustand über, es entsteht Wasserdampf. Misst
man die Temperatur, so bemerkt man, dass diese konstant bei 100°C bleibt,
so lange ein Wasser-Wasserdampf-Gemisch vorliegt. Diese Temperatur
nennt man die Siedetemperatur des Wassers.
Durch Zuführung von Wärmeenergie (erhitzen), kann man also die Übergänge
von fest zu flüssig (schmelzen) und von flüssig zu gasförmig (verdampfen)
erreichen.
Wasserdampf kondensiert sehr leicht an kalten Fensterscheiben und Wänden.
Der Übergang von gasförmig zu flüssig (kondensieren) ist also durch
Entzug von Wärmeenergie (abkühlen) möglich.
Ebenso kann man den Übergang von flüssig zu fest (erstarren) erreichen,
indem man Wasser im Tiefkühlfach durch Wärmeentzug gefrieren lässt.
Versuch 2:
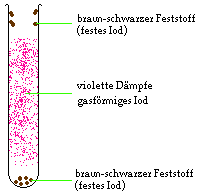 |
Durch Erhitzen von Iod (braun-schwarzer Feststoff) entstehen violette Dämpfe
(gasförmiges Iod). Am kühleren oberen Teil des Reagenzglases kann man
denselben braun-schwarzen Feststoff erkennen wie am Boden des Reagenzglases. Wenn man also den Feststoff Iod erhitzt, kann man den Übergang von fest zu flüssig nicht feststellen, es findet durch Zufuhr von Wärmeenergie sofort der Übergang von fest zu gasförmig statt (sublimieren). Im oberen Teil des Reagenzglases kann man nur den Übergang von gasförmig zu fest beobachten (resublimieren). Durch Entzug von Wärmeenergie findet sofort der Übergang von gasförmig zu fest statt. Für verschiedene Stoffarten gibt es also nur die zwei Aggregatzustände: fest und gasförmig. Bemerkung: Ein Aggregatzustand besteht nur für eine Stoffportion, also für eine große Anzahl von Teilchen. Ein einzelnes Teilchen kann nicht in verschiedenen Aggregatzuständen vorkommen. |